УДК 616.441.001.3
300026, Тула, пр. Ленина, 108, НИИ новых медицинских технологий, лаборатория онкологии; лаборатория технического сопровождения хирургических технологий; тел./факс: (0872) 33-22-09;
E-mail: niinmt@mednet.com
Отмечаемый многими авторами рост заболеваемости злокачественными опухолями различных локализаций относится и к раку щитовидной железы [6]. Причем этот рост выражается в увеличении числа заболевших как старшего, так молодого возраста и связан с воздействием ряда экзогенных факторов, таких как повышенная ионизация атмосферы, облучение области головы и шеи, длительное применение при лечении доброкачественных образований щитовидной железы (ЩЖ) антитиреоидных препаратов и радионуклидов. На долю рака ЩЖ приходится 1,5-2% всех злокачественных опухолей, кроме того, отмечается тенденция роста частоты этого заболевания [3, 7, 11]. По данным ВОЗ за последние 20 лет заболеваемость раком ЩЖ удвоилась в основном за счет лиц молодого и среднего возраста. При раке ЩЖ преобладают дифференцированные формы новообразований, протекающие относительно благоприятно, поэтому смертность в 2-3 раза ниже по сравнению с заболеваемостью. Рак ЩЖ развивается медленно, и в некоторых случаях (примерно 4,2%) при клинически неизмененной железе только рутинное посмертное изучение органа выявило скрытый рак [6].
Сложность диагноза злокачественной опухоли ЩЖ подтверждается статистикой: примерно в 50% случаев у больных раком ЩЖ устанавливается ошибочный диагноз, причем у 60% больных наблюдается III и IY стадии заболевания [2, 4, 6], на начальных же стадиях болезни ошибки диагностики составляют 50-100%. По сводным данным зарубежной литературы при этом заболевании правильный дооперационный диагноз устанавливается лишь в 18-33% случаев.
Ошибки диагностики рака ЩЖ связаны, в первую очередь, с многообразием его форм и проявлений и, в ряде случаев, со скрытым и бессимптомным протеканием опухолевого процесса. В настоящее время диагностика рака ЩЖ главным образом основывается на клинических данных, при этом следует учитывать, что в анамнезе отсутствуют специфические ранние симптомы, так как на начальных стадиях рак не имеет ни одного патогномоничного признака болезни, и характер опухоли скорее подозревается, чем может быть распознан. В поликлинике Онкологического научного центра РАМН применяется комплексная диагностика [6], включающая в себя пункцию опухоли ЩЖ и увеличенных лимфатических узлов, рентгенологическое исследование, сцинтиграфию с радиоактивным йодом. Пункция опухоли позволяет установить окончательный диагноз у 55-90% больных на основании цитологического исследования, появляется возможность диагностирования непальпируемого рака ЩЖ посредством изучения гистологического строения опухоли и исключения других заболеваний [9].
От результатов цитологической диагностики во многом зависит выбор наиболее рационального лечения [6, 10, 11]. Перед морфологической диагностикой стоят две основные задачи: идентификация злокачественной опухоли, уточнение структуры и гистогенетической природы опухоли.
Пункцию выполняют тонкой иглой по разным методикам, проводят набор биоптата, после чего пунктат аспирируют. Многочисленные работы, посвященные цитологической диагностике новообразований различных локализаций, выполненные на обширном клиническом материале, доказали безопасность и высокую эффективность пункционного метода, а ряд экспериментальных данных указывает на отсутствие проблемы имплантации и усиления метастазирования в результате нарушения целостности ткани при пункции опухоли [6].
Эффективность пункционного метода зависит от полученного материала, правильности выбора места для пункции, способа взятия биоптата. Совпадение результата цитологического анализа при раке ЩЖ с реальным состоянием составляет 55,7-93,2% [3, 6]. Достоверность метода можно увеличить, если пунктирование проводить под контролем ультразвукового исследования [6]. Однако при пунктировании следует учитывать богатое кровоснабжение ЩЖ, что осложняет исследования. Тем не менее, использование цитологического метода в ОНЦ РАМН, в процессе которого забор материала производится без аспирации, позволяет в 96% случаев правильно охарактеризовать первичный процесс в ЩЖ как злокачественный, а в лимфатических узлах - в 93,4%, установить гистологическое строение опухоли в 78% случаев [1, 6]. Ограничением в ряде случаев являются малые размеры первичного очага при скрытом раке.
Некоторые авторы [3] рекомендуют проводить аспирационную пункцию при злокачественных опухолях ЩЖ. Но при этом абсолютно не учитывается, что аспирация ведет к разбавлению пунктата кровью, что, в свою очередь, затрудняет исследования. Коме того, установлено, что аспирационная пункция по своей информативности не превосходит обычную пункционную биопсию.
Техническая сторона выполнения пункции оказывает влияние на качество клинического диагноза. Как указывалось выше, предпочтительнее забор материала для цитологического исследования производить без отсасывания шприцем. При этом разработка новых технологий биоптата должна проводиться с учетом гистологического строения опухоли ЩЖ. Щитовидная железа окружена соединительнотканной капсулой, прослойки которой направляются вглубь и разделяют орган на дольки. Структурно-функциональными единицами ЩЖ являются фолликулы - шаровидные образования с полостью внутри. В просвете фолликула - коллоид - секреторный продукт эпителиальных клеток, составляющих выстилку фолликула. При жизни коллоид представляет собой вязкую жидкость, состоящую, в основном, из тироглобулина. Фолликулы разделяются прослойками рыхлой волокнистой соединительной ткани. В этих же прослойках обнаруживаются компактные скопления тиреоидных эпителиальных клеток. Разграничение гиперпластических и опухолевых процессов в ЩЖ труднее, чем в других органах и тканях из-за того, что такие постоянные признаки бластомогенеза, как клеточный атипизм и митотическая активность, далеко не всегда присущи злокачественному росту применительно к ткани ЩЖ, равно как и наооборот: их отсутствие не исключает его [5]. Наибольшие расхождения получены при папиллярном раке (7%) [6]. При заборе биоптата важно сохранение, хотя бы частичное, структуры опухоли.
Существует способ забора биоптата [8], который выполняется иглой, имеющей расположенные вдоль оси иглы отверстия на боковой поверхности трубки иглы. Отверстия в поперечном сечении имеют сегментообразную форму, причем противоположные кромки отверстий закручены по спирали; одна из кромок выступает над наружной поверхностью трубки и выполнена режущей, а другая кромка загнута по спирали внутрь трубки и является направляющей. Иглу поступательным движением с незначительным вращением вокруг своей оси в сторону, противоположную режущим кромкам, проводят к исследуемому участку опухоли. Затем иглу вращают вокруг своей оси в направлении, совпадающем с направлением режущих кромок; при этом срезанная ткань поступает внутрь иглы. Далее игла извлекается и биоптат вымывают из просвета иглы. При этом структура опухоли не сохраняется и поэтому трудно определить локализацию отдельных участков.
Для упрощения процесса взятия биоптата был разработан способ пункционной биопсии, при котором взятие пробы осуществляют с сохранением структуры биопсийного материала при дозированном прерывании процесса его набора; набор биопсийного материала осуществляют с началом его извлечения из тканей, а прерывание процесса набора биопсийного материала производят без прерывания процесса его извлечения из тканей.

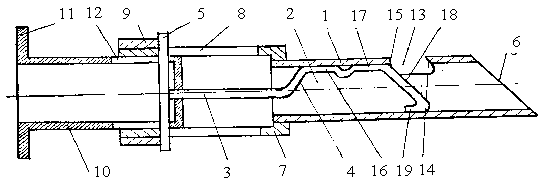
Рис. 1. Схема расположения
элементов иглы для пункционной биопсии в исходном положении перед
пункцией, где 1 - трубка, 2 - сквозная полость, 3 - мандрен, 4
- упругий стержень, 5 - ручка, 6 - рабочий конец, 7 - канюля,
8 - сквозной паз, 9 - ограничительное кольцо, 10 - позиционер,
11 - втулка, 12 - паз втулки, 13 - окно на боковой поверхности
трубки, 14 - режущая кромка, 15 - нережущая кромка, 16 - запорный
выступ, 17 - выступ, 18 - торцевая поверхность стержня, 19 - уступ
Игла для пункционной биопсии содержит трубку 1 со сквозной полостью 2, в которой расположен с возможностью продольного перемещения упругий мандрен 3.
Мандрен состоит из упругого стержня 4, соединенного с ручкой 5. На трубке 1 имеется заостренный рабочий конец 6, а на противоположном конце трубки 1 закреплена канюля 7. На боковой поверхности канюли 7 выполнен сквозной паз 8 и закреплено ограничительное кольцо 9. В полости канюли 7 расположен с возможностью продольного перемещения позиционер 10, выполненный в виде кинематической пары пятого класса, например, втулки с буртиком 11 и сквозным пазом 12. Ручка 5 мандрены 3 расположена в пазах 8 (канюли 7) и 12 (позиционера 10) с возможностью фиксированного продольного перемещения в пазах. На боковой поверхности трубки 1 выполнено отверстие 13 в виде окна, одна часть которого имеет режущую кромку 14 в форме ласточкиного хвоста, расположенную со стороны заостренного рабочего конца 6, а другая часть окна 15 имеет атравматичную форму, например, закругления на кромках пересечения нережущей части 15 отверстия 13 с наружной поверхностью трубки 1. На упругом конце стержня 4 мандрена 3 имеются два выступа 16 и 17, совпадающие по форме с отверстием 13 и выполненные с возможностью последовательного взаимодействия с последним. При совмещении выступа 16 стержня 4 с отверстием 13 торцевая поверхность 18 стержня 4 совпадает по форме с заостренным концом 6 трубки 1. На конце стержня 4 выполнен упругий уступ 19, взаимодействующий с внутренней поверхностью полости 2 трубки 1.
Перед употреблением иглу стерилизуют, как обычные хирургические инструменты. Для взятия биологической ткани на гистологический анализ производят соответствующую обработку выбранного участка кожи и проводят рабочий конец иглы 6 непосредственно в зону биопсии. Предварительно мандрен 3 устанавливают в полости 2 трубки 1 в исходное положение (рис. 1), при этом ручка 5 мандрена 3 располагается в пазу 8 канюли 7 в правом крайнем положении, торцевая поверхность 18 стержня 4 совпадает с заостренным рабочим концом 6 трубки 1 и выступ 16 стержня 4 совпадает с заостренным рабочим концом 6 трубки 1, а выступ 16 стержня 4 закрывает отверстие 13 на боковой поверхности трубки 1. Позиционер 10 находится в исходном положении, упираясь буртиком 11 в торец ограничительного кольца 9, закрепленного на канюле 7. При введении иглы окружающие ткани не попадают в полость 2 трубки 1, т. к. они отжимаются выступом 16 от режущей кромки 14 отверстия 13 и не травмируются нережущей частью 15 отверстия 13. После подведения иглы к месту взятия пробы позиционер 10 переустанавливают в канюле 7 в крайнее левое положение, при этом ручка 5 мандрена 3 устанавливается в крайнем левом положении в пазу 8 канюли 7; торцевая поверхность 18 стержня 4 занимает положение в полости 2 трубки 1 позади отверстия 13, открывая доступ биопсийному материалу в полость 2 трубки 1 (рис. 2), после чего начинается процесс извлечения иглы из ткани, параллельно с которым идет набор биопсийного материала. При этом режущая кромка 14 отверстия 13 срезает ткань и направляет ее в полость 2 иглы. Для прекращения набора биопсийного материала, не прерывая поступательного движения иглы, позиционер 10 возвращают в исходное положение (рис. 3). При этом мандрен 3 остается неподвижным относительно трубки 1 до тех пор, пока паз 12 позиционера 10 своей левой стенкой упрется в ручку 5, после чего позиционер 10 совместно с мандреном 3 продолжают перемещать в правое конечное положение до упора буртиком 11 позиционера 10 в торец ограничительного кольца 9. В этом положении выступ 17 упругого стержня 4 закрывает отверстие 13, слегка приподнимаясь за счет упругости уступа 19 над режущей кромкой 14 отверстия 13, что препятствует травмированию окружающих тканей при дальнейшем извлечении иглы. После выведения иглы для выемки биопсийного материала из полости 2 трубки 1 мандрен 3 за ручку 5 перемещают в пазу 8 канюли 7 в правое конечное положение. При этом торцевая поверхность 18 стержня 4 выталкивает биопсийный материал за пределы рабочего конца 6 трубки 1.
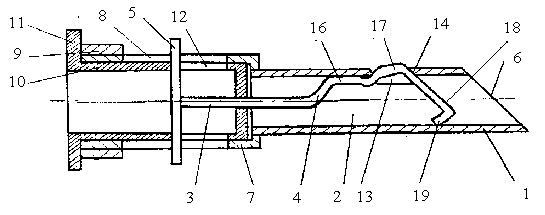
Предлагаемый способ пункционной биопсии и конструкция иглы позволяют осуществить биопсию тканей независимо от их консистенции, при этом упрощается процесс пункции ткани и обеспечивается хорошее качество микропрепаратов. Вследствие того, что стенки иглы имеют минимальную толщину, обусловленную требованиями прочности, и режущая кромка совершает только поступательное движение, повышается сохранность структуры биопсийного материала за счет изолированного его извлечения из окружающих тканей.
Моделирование работы пункционной иглы предлагаемой
конструкции подтвердило работоспособность рассмотренного способа
забора биоптата, при этом не наблюдалось нарушения структуры пробы.
В настоящее время отрабатывается конструкция.
1. Валдина Е.А., Пучков Ю.Г. Пункционная биопсия в диагностике заболеваний щитовидной железы // Вестн. хир.- 1988, ¦ 10.- С.154-155.
2. Гинзбург Г.А. и др. Современные принципы диагностики и лечение рака щитовидной железы (информационное письмо).- Свердловск, 1986.- С. 28.
3. Мышкин К.И., Амирова Н.М., Чернышев Н.В. Проблемы и итоги хирургического лечения при раке щитовидной железы // Актуальные вопросы диагностики и лечения злокачественных опухолей головы и шеи.- М., 1991.- С. 130-132.
4. Панов Е.Д. Ошибки в диагностике и лечении рака щитовидной железы // Сов. мед.- 1987, ¦ 8.- С. 98-101.
5. Патологоанатомическая диагностика опухолей человека: Руководство в 2-х томах. Т. 2.- М.: Медицина, 1993.- С. 688.
6. Пачес А.И., Проин Р.М. Рак щитовидной железы // Центр внедрения достижений науки и техники.- М., 1995.- С. 370.
7. Пинский С.Б., Кругляков И.М., Рыжков О.В. Современные возможности диагностики щитовидной железы // Актуальные вопросы диагностики и лечения злокачественных опухолей головы и шеи.- М., 1991.- С. 102.
8. Селезнев К.Г. и др. Игла для пункционной биопсии. Авт. свид. ¦ 1519656, СССР, опубл. Бюл. ¦ 41, 1989.
9. Трапезников Н.Н., Шайн А.А. Онкология.- М.: Медицина, 1992.- 400 с.
10. Block M. Primary treatment of well differentiated thyroid caneer // J. Surg. Oncol.- 1981.- Vol. 16, ¦ 3.- P. 279-288.
11. Sherman C.Ir. Thyroid Cancer. Manual
of Clinical Oncology // Fifth Edition Vicc.- 1990.- P. 204-210.
The method and needle construction are suggested for thyroid punch biopsy. The needle has minimal thickness of the wall and its cutting edge carries out only progressive motion, that allows to conserve the bioptic material structure due to its isolation from surrounding tissues during extraction.