Системный анализ биохимических характеристик этапов доклинического периода хронических болезней
нижних дыхательных путей
В.Е. Рождественский*,
В.И. Спинов**, Н.В. Юргель**
1. Введение
Хронические
болезни нижних дыхательных путей (ХБНДП), хронический бронхит (ХБ) и бронхиальная
астма (БА), составляют группу наиболее распространенных болезней внутренних органов. ХБ и БА обеспечивают
максимальное число случаев временной нетрудоспособности и инвалидизации
у пульмонологических больных. По современным представлениям, ХБ относят к
группе хронических обструктивных заболеваний легких
(ХОЗЛ), а БА выделяют из этого списка.
Имеются, однако,
общие черты, позволяющие объединить эти два заболевания в группу ХБНДП. Прежде всего,
это - наличие воспаления бронхиального дерева, его гиперчувствительность
к экзогенным воздействиям, возможность взаимоперехода
(формирование БА у больных ХОЗЛ и исход БА в ХОЗЛ). Сказанное позволяет
предполагать наличие общих для этих заболеваний неспецифических механизмов резистентности и формирования патологического процесса
[1].
Одним из
ключевых механизмов неспецифической резистентности
является свободно-радикальное окисление липидов
(СРОЛ), роль которого в развитии патологических изменений интенсивно изучается [2].
Известная роль белков "острой фазы": a1-антитрипсина
(a1АТ)
и церулоплазмина (ЦП)
в формировании воспаления недостаточно
изучена во взаимосвязи со свободно-радикальными
процессами.
Цель
исследования - охарактеризовать активность свободно-радикального
окисления (СРО) и белков "острой фазы" на 4-х этапах маршрута развития ХБНДП
[3], существование которых подтверждено функциональными исследованиями [4].
2. Материал и методы исследования
Обследовано
98 индустриальных рабочих с различными сочетаниями факторов риска ХБНДП в возрасте 19-53 лет и 10 больных ХБНДП. Группа контроля - 35
человек в возрасте 18-53 лет с факторами риска развития ХБНДП, не
подвергавшихся воздействию промышленных поллютантов и
не имевших отклонений функции внешнего дыхания. Число наблюдений по методикам -
не менее 15.
Использовали
ряд биохимических методик [5]. Из плазмы крови готовили липидный экстракт для
определения оснований Шиффа (ШО) по количеству липофусциноподобного пигмента, диеновых коньюгат
(ДК) - гидроперекисей липидов и общих липидов. Определяли активность a1АТ
и ЦП [1]. Количество последнего выявляли
атомно-абсорбционным определением меди (Cu).
Помимо ЦП - основного внеклеточного антиокислителя - определяли активность
каталазы (КА) периферической крови -
одного из ключевых ферментов клеточной антиокислительной
активности (АОА).
Для
установления взаимодействия с клеточным звеном изучали показатель
макрофагальной трансформации моноцитов периферической крови (МТМ) [1]. Полученные результаты сравнивали по группам с
применением критерия t-Стьюдента. В последующем проводили системный
анализ в моделях, связывающих рассчитанный индекс риска развития ХБНДП с
биохимическими параметрами и расчетом устойчивости сформированных моделей по
уравнению[6]:
![]()
где b0,
bi
- коэффициенты регрессии; xi - независимые переменные (биохимические параметры).
Т.о., были сформированы модели в каждой из
четырех групп риска и у больных ХБНДП с базовым показателем численного
выражения степени риска, связанного с результатами биохимических исследований,
характеризующими ШО, ДК, КА, a1АТ, ЦП, Cu.
Системный анализ проведен ретроспективно. Это
не обеспечило в полной мере идентичных моделей в каждой из групп риска, но
обусловило выбор высокого ценза значимости (r³0,7). Разнонаправленность корреляционных
связей изображена в моделях расположением вверх (+)
или вниз (-), а численные значения для отдельных параметров - слева направо по
убыванию.
3. Результаты
Как видно по
данным табл. 1, количество промежуточных продуктов перекисного окисления
липидов - ДК - достоверно не отличалось от контроля во всех группах риска. В то
же время количество конечных продуктов СРОЛ - ШО во всех группах риска было
достоверно увеличено (p < 0,05). Активность
каталазы, начиная с группы риска 2, достоверно увеличена (p
< 0,05), в группе риска 3 (p < 0,01)
различия нарастали, а в группе риска 4 их не отмечалось. Количество меди
сыворотки во всех группах было достоверно увеличено (p
< 0,001). Не отмечалось достоверных различий при изучении оксидазной активности ЦП
ни в одной из групп. Другой белок "острой фазы" - a1АТ,
начиная с группы риска 2, достоверно возрастал (p
< 0,01); достоверность увеличивалась в группах риска 3 и 4 (p < 0,001). Не отмечалось достоверных различий
между группами риска ни по одному из изученных параметров.
Таблица
Показатели
биохимических исследований в группах риска развития ХБНДП в сравнении с
контролем, М+m
|
Показатели |
Контроль |
Группы риска |
|||
|
1 |
2 |
3 |
4 |
||
|
ДК, мэкв×мг-1 липидов |
0,39+0,04 |
0,36+0,04 |
0,33+0,03 |
0,29+0,06 |
0,31+
0,05 |
|
ШО, ед. фл.
мг-1 липидов |
8,02+0,82 |
12,8+2,01* |
16,5+1,8* |
17,4+2,8* |
15,1+2,9* |
|
Cu, мкг×мл-1 |
0,35 +0,03 |
0,55+0,03*** |
0,58+0,05*** |
0,68+0,05*** |
0,9+
0,09*** |
|
КА, ед×г-1 ×мин-1 |
0,48+0,01 |
|
1,63+0,46* |
1,6+ 0,33** |
0,92+
0,51 |
|
ЦП, мкмоль×мл-1×мин-1 |
2,30+0,17 |
1,93+0,58 |
2,04+
0,28 |
2,30 +
0,38 |
2,7+
0,57 |
|
a1АТ, мг×мл-1×мин-1 |
12,21+0,46 |
12,12+1,2 |
15,7+
0,69** |
16,4+ 0,7*** |
16,6+ 0,9*** |
Примечание:
число наблюдений по методикам 55-98.
Таким
образом, при исследовании биохимических
показателей, начиная с группы 1, наблюдалось нарастание активности СРОЛ по
конечным продуктам (ШО) и увеличение содержания меди в сыворотке. Последнее
свидетельствовало о напряженности антиокислительных
факторов, среди которых основным является ЦП. Начиная со второй группы риска увеличивалась активность антиокислительного
фермента КА, что сохранялось в 3-й группе, а в 4-й - достоверность различий
терялась. Последнее, вероятно, свидетельствует об
истощении антиокислительных механизмов после периода
напряжения. Повышение активности важнейшего ингибитора протеаз a1АТ
отражало напряженность в системе "протеазы - ингибиторы", начиная со второй группы.
Один из факторов воспаления - ЦП, не выявляя достоверных различий с контролем
ни в одной из перечисленных групп, показал низкую информативность при развитии
ХБНДП, что, вероятно, было связано с токсическими воздействиями промышленных поллютантов.
По результатам
биохимических исследований, отмечалась повышенная напряженность в системе "СРОЛ
- антиоксиданты" с 1 группы риска, а со второй группы присоединилась напряженность
в системе "протеазы - ингибиторы". Сохранение пропорциональных соотношений в последней свидетельствуют
о невысокой токсичности
продуктов СРОЛ по отношению к белковым структурам, что обеспечивается
достаточной антиоксидантной защитой. Тем не менее, не
исключается развитие липидных повреждений
на уровне клеточных мембран эндотелия и форменных элементов периферической
крови. К этому же приводит нарастание протеазной
емкости, хотя и уравновешенное увеличением активности ингибиторов.
Несовершенство критерия t-Стьюдента
привело к необходимости системного анализа по описанным выше принципам.
Модель 1
выдержала ценз (рис. 1, r = 0,94), а
показатели ШО, ДК и ЦП имели отрицательные корреляционные связи с индексом
риска.
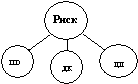
Рис. 1.
Соотношения в биохимической модели:
группа риска
1, r
= 0,94
Отрицательная связь характеристик СРОЛ (ШО, ДК) и ЦП со степенью риска
развития заболевания свидетельствовала, прежде всего, о многообразии
воздействий производственной среды на макроорганизм,
наличии в связи с этим определенных биохимических изменений, а также о
достаточно высокой противоинфекционной защите,
обеспечиваемой активизацией СРОЛ. Следует
предполагать, что отмеченные изменения не выходят за рамки адаптации у лиц,
испытывающих воздействие агрессивных профессиональных факторов, и имеют саногенетическое значение, отражаемое высокой устойчивостью
модели.
Оценка
взаимосвязей в значимой биохимической модели во 2-й группе риска (рис. 2, r = 0,81) выявила преимущественную связь
степени риска с функциональной активностью a1АТ. Связь
эта положительная. Установлена слабая отрицательная связь степени риска с
показателями ДК и ШО.
Предполагается
преимущественное нарушение равновесия протеиназы -
ингибитора, так как промежуточные продукты ДК стимулируют активность a1АТ,
а конечные ШО влияют на деградацию последнего. Относительное снижение
устойчивости модели до r = 0,81 указывает на чувствительность к воздействию промышленных поллютантов.
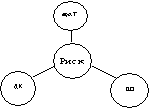
Рис. 2. Соотношения показателей в биохимической
модели: группа риска 2, r = 0,81
В 3-й группе
риска низкая сопряженность рассматриваемой модели заставила нас включить
показатель МТМ, имевший положительную корреляционную связь со степенью риска.
Тем не менее, модель не выдержала установленного ценза (рис. 3, r = 0,56), отражая значительное снижение саногенетических механизмов.
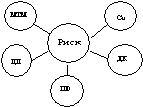
Рис. 3. Соотношения в биохимической модели:
группа риска 3, r = 0,56
Модель,
характеризующая биохимические показатели в 4-й группе, оказалась недостаточно
статистически значимой (рис. 4, r = 0,67). Однако все показатели и, особенно, МТМ
положительно коррелировали с признаком степени риска.
Следует отметить нарастающую по сравнению с группой риска 3 положительную связь
показателя МТМ, а также положительные связи показателей процесса СРОЛ и Cu (количество ЦП).
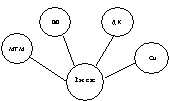
Рис. 4. Взаимосвязи показателей биохимической модели:
группа риска 4, r = 0,67
Т.о., в 4-й группе
риска развития ХБНДП отмечено возобновление сопряженности составленных плеяд по
сравнению с группой 3. Это происходит, по-видимому, от дополнительных
воздействий факторов риска. Возможно, одним из главенствующих
в числе последних является инфекционный [6].
![]()
Рис. 5. Взаимосвязи показателей ПОЛ и каталазы.
Больные ХБНДП, r = 0,7
В группе больных ХБНДП при отсутствии рассчитанного риска устанавливались
взаимосвязи между показателями. Модель биохимических показателей, сформированная по отношению к ДК
как к базовому, отразила положительную связь с ШО и отрицательную с активностью
каталазы (рис. 5, r
= 0,7), что свидетельствовало о преобладании активности СРОЛ над антиокислительной активностью. Степень сопряженности модели, превышая
таковую в группах риска 3 и 4, не достигала интенсивности, отмеченной во 2-й
группе.
Т.о., изменения соотношений продуктов СРОЛ, антиокислителей
и белков "острой фазы" с численными значениями индивидуального индекса риска на
этапах доклинического периода ХБНДП позволили установить динамику устойчивости
(сопряженности) рассмотренных моделей, в которых сопоставлены организменный и молекулярно-радикальный
уровни системной организации.
Условная динамика при сопоставлении моделей по
этапам развития ХБНДП (рис. 6) выявила саногенетическое
значение изученных биохимических характеристик в 1-й и 2-й группах с
последующим истощением адаптационного потенциала в 3-й группе. Повышение устойчивости (сопряженности) в 4-й и в группе
больных позволяет говорить о патогенетическом значении СРОЛ и белков "острой
фазы" после этапа перестройки неспецефической резистентности.
Проведенный системный анализ отразил роль СРОЛ в динамике формирования
ХБНДП. После консолидации показателей в группе 1 за счет внешних
агрессивных воздействий, наблюдалось отступление саногенеза во 2-й и 3-й группах. Дальнейшее восстановление
устойчивости позволяет предположить переключение физиологических механизмов на
патогенетические, что наблюдалось, начиная с группы 4, где формируется
хронический воспалительный процесс. Он опережает клинические проявления,
которые наблюдаются лишь в группе больных. При переходе от сано- к патогенезу сказывалась
токсическая роль СРОЛ. АОА была недостаточна, и подавление ингибитора протеаз
соответствовало модификации клеточных мембран, что проявилось нарастанием МТМ.
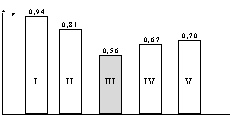
Рис. 6. Устойчивость моделей биохимических показателей в динамике развития ХБНДП
Т.о., этапы формирования ХБНДП характеризуются различными соотношениями
биохимических показателей, отражающими последовательность адаптации и истощения изученных
составляющих метаболизма. Третий этап (ранняя предболезнь) характеризуется значительным снижением
неспецифической резистентности за счет ее
рекомбинационных преобразований. Четвертый
этап (поздняя
предболезнь) характеризуется как донозологическое
воспаление. СРОЛ и белки "острой фазы" на этапах 1 и 2 связаны между
собой саногенетически, тогда как на этапах 3, 4 и у
больных ХБНДП СРОЛ имеет патогенетическое значение и токсично для ЦП и a1АТ. Мембраномодифицирующее действие СРОЛ
проявляется, начиная с этапа 3, увеличением МТМ.
Литература
1.Рождественский М.Е. Ранняя
диагностика и прогнозирование хронических неспецифических заболеваний легких:
Сер. Профилактическая пульмонология.- Ч. I.- Омск, 1998.- 84 с.
2. Владимиров Ю.А., Арчаков А.И. Перекисное
окисление липидов в биологических мембранах.- М.: Наука, 1972.- 196 с.
3. Доронин В.П., Рождественский М.Е. // ВНМТ.- 1998.-
Т. 5., N2.- С.108-110.
4. Рождественский М.Е., Юргель Н.В. //
ВНМТ.- 1998.- Т. 5, N 3-4.- С. 63-66.
5. Головин А.А., Рождественский М.Е., Шадевский
В.М. // ВНМТ.- 1996.- Т. 3, N3.- С. 59-60.
6. Рождественский М.Е. Методология диагностики доклинического
периода хронических неспецифических заболеваний легких.- Сер. Профилакт. пульмонол..- Ч. II.- 2000.- Омск.- 82 с.
A System Analysis of
Biochemical Characteristic of Stages of a Preclinical Period of Chronic
Diseases of the LowerRespiratory Tract
V. E. Rozhdestvenskiy,
V. I. Spinov, N. V. Yurgel'.
Summary
The authors creat
an own theory of stage of a preclinical period of chronic diseases of the lower
respiratory tract and substantiate it by a system analysis of biochemical
research findings, i.e., free-radical oxygenation of lipids and albumins of "an
acute stage". On the base of the research the authors describe the 3rd
stage of recombinational transformations of
nonspecific resistance. The 4th stage is defined as prenosologic inflammation.
Key words: lower respiratory tract, prenosologic inflammation